全球范围内甲状腺癌患病人数不断攀升,年发病数已从2000年的12.3万[1]上升至2020年的58.6万[2],20年间增长了4.77倍,成为了“流行病”。相比之下甲状腺癌死亡率则维持在较低水平[3]。乳头状癌(PTC)是甲状腺癌最常见的病理类型[4],全球范围内甲状腺癌发病率增加主要归因于PTC增加[5]。以1974~2013年间美国统计数据为例,PTC及微小癌(肿瘤直径≤1.0cm)增速最高[6]。
高发病率背景下相对较低的死亡率,以及疾病谱向PTC和微小癌转变,引发了学术界对甲状腺癌 “过度诊疗” 的争议,也为临床医生带来一些困惑。那么,应该如何理解不同国家指南以及真实世界诊疗上的差异呢?本文特邀华中科技大学附属协和医院黄韬教授展开细致解读,现将内容整理如下。

黄韬 教授,华中科技大学附属协和医院
博士研究生导师
华中科技大学附属协和医院外科教研室主任、乳腺甲状腺外科主任
中国医促会普通外科学分会主任委员
中国医师协会外科医师分会甲状腺外科医师委员会副主委
中国研究型医院学会甲状腺疾病专业委员会副主委
中国研究型医院学会甲状腺疾病专业委员会临床研究学组组长
中华医学会外科学分会甲状腺及代谢外科学组委员
中华医学会肿瘤学分会甲状腺肿瘤专业委员会委员
中国抗癌协会甲状腺癌专业委员会常委
中国抗癌协会乳腺癌专业委员会委员
湖北省临床肿瘤学会甲状腺癌专委会主委
湖北省抗癌协会甲状腺癌专委员会副主委
♦ 甲状腺癌管理:美国指南已出现诊疗降级趋势,其他国家仍相对积极
◊ 甲状腺微小癌的诊断:欧美趋于保守,中日韩英更积极
2015年美国ATA指南推荐:超声高度怀疑恶性的结节行细针穿刺活检(FNA)的指征是肿瘤直径≥1.0cm,较之前阈值有所提高,有诊断降级倾向 [7,8]。
与美国一致,欧洲指南[9]也不建议对≤1.0cm的结节行FNA。这实际可能限制和减少了对微小癌的诊断,是否意味着即使超声高度怀疑恶性,微小癌也不推荐穿刺评估,不需要诊断?中国[10]、日本[11]、韩国[12]则将FNA阈值定为0.5cm,英国[13]建议若临床怀疑淋巴结转移即使结节≤1.0cm也应行FNA,对微小癌诊断更为积极。

表1 各国指南对≤1cm甲状腺结节FNA的推荐意见
注:ATA=美国甲状腺学会,ESMO=欧洲肿瘤内科学会,CATO=抗癌协会甲状腺癌专业委员会,KTA=韩国甲状腺学会,JTA=日本甲状腺学会
◊ 甲状腺微小癌的管理:美国将主动监测加入推荐
2022年美国国立综合癌症网络(NCCN)指南[14]推荐:FNA疑诊PTC患者,若肿瘤直径≤1.0cm且颈部超声未发现淋巴结转移(cN0),可以选择主动监测(active surveillance),也可选择甲状腺腺叶切除术。但时至今日,仅有低质量循证医学证据支持主动监测用于低危PTMC,且其可操作性存疑。
◊ 1~4cm DTC的手术范围:美国趋于保守,日韩更积极
ATA指南[8]推荐:1~4cm分化型甲状腺癌(DTC)如果经临床评估未发现淋巴结转移(cN0)和腺外侵袭证据,初始手术方式可选择甲状腺全切/近全切除术或甲状腺腺叶切除术;对于低危DTC,腺叶切除可能就已足够。
韩国指南[12]则认为1~4cm DTC无淋巴结转移和腺外侵袭的情况非常少见,全切对于此类患者几乎是必须的;而且韩国外科医生的手术量普遍较高,手术并发症发生率低于其他国家;综上所述,建议在全/近全切和腺叶切除中灵活选择[12]。日本指南[15]则将行甲状腺全切术的肿瘤界值确定在2cm。
综上所述,在 “过度诊疗” 背景下,美国指南对甲状腺癌诊断与治疗的推荐已趋于保守,而英国、韩国、中国则相对积极,是什么原因造成了这种差异?回顾各国甲状腺癌治疗效果的演变历程,或许能找到答案。
♦ 以史为鉴,强调甲状腺癌“过度诊疗”为时尚早
◊ 美国:疗效更早接近极限,治疗降级后隐忧初现
1940~1949年间,美国甲状腺癌的5年相对生存率仅为64%[16],受限于有限的检测手段,此时期接受外科手术的患者普遍分期晚、肿瘤较大或已出现广泛颈部转移、远处转移;同时手术范围通常较为保守,在切除肉眼可见的癌灶同时尽可能保留剩余甲状腺。
1950年后,人们逐渐认识到不彻底的手术将增加肿瘤残留风险,增加复发和死亡率,故而开始引入甲状腺全切术、甲状腺腺叶切除术、颈部淋巴结清扫等术式。1965~1969年,美国甲状腺癌5年生存率提升至84%。
1970年开始,Mazzaferri等众多学者开始探索术后放射性碘治疗、TSH抑制治疗在改善DTC预后方面的价值[17]。分析1985~1995年美国国家癌症数据库(NCDB)[18]中5.3万例病例资料发现,DTC患者接受标准甲状腺手术(甲状腺全/近全切除术或腺叶切除术)的比例已近80%,全切术后放射性碘治疗比例达到38.3%,此时PTC、FTC的5年相对生存率已分别达到96%、91%。可见随着诊疗技术和规范性的提高,美国甲状腺癌疗效更早接近极限。
诊疗降级是否会影响甲状腺癌预后?分析2000-2017年美国加州6.9万甲状腺癌登记数据[19]发现,2014年后PTC、未分化癌、局部扩散及转移癌、大癌的年死亡率均呈增长态势(图1)。这是否是2009年ATA指南的5年后效应?2015年ATA指南又会对甲状腺癌的生存率和死亡率产生什么影响?仍需长时间观察。
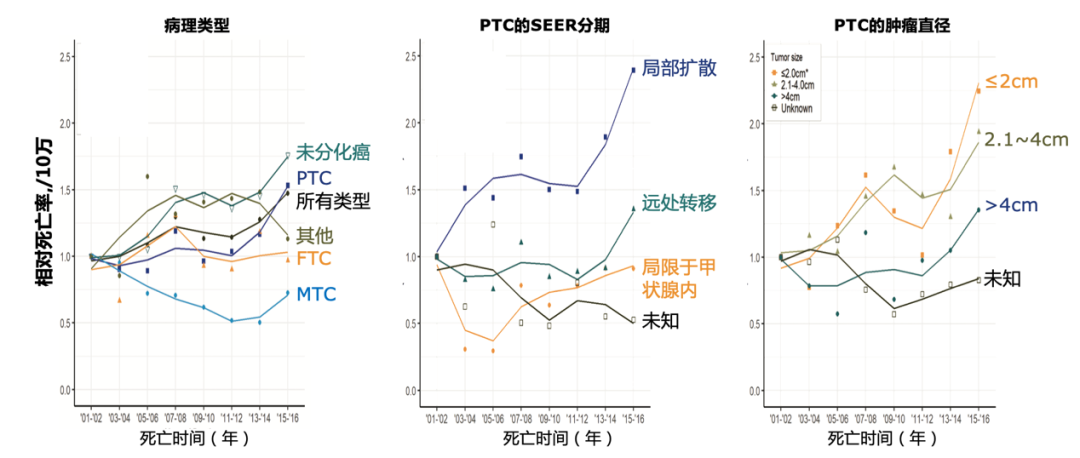
图1 2001~2016年甲状腺癌年死亡率变化趋势(来源:美国加州肿瘤登记数据库)
◊ 韩国:从积极诊疗中获益更大
1999年,韩国政府发起一项全民免费肿瘤筛查项目,由于颈部超声价格低廉,很多医院将甲状腺癌超声筛查加入筛查套餐[20]。这一举措导致2000年以后韩国确诊甲状腺癌人数迅速上升,2011年相比1993年发病率升高的15倍,引发对“过度诊断”争议。但韩国筛查真的没有获益吗?
回顾韩国流行病学数据发现:从开展筛查项目5年后(也就是2005年)开始,甲状腺癌特异性死亡率开始下降[21];2003~2015年死亡率的APC约下降4.3%[22]。
从肿瘤分期来看,筛查不仅检出了更多微小癌,也提高了大癌、淋巴结转移和转移癌的检出率[23]。确诊时肿瘤直径从1999年的2.15cm降低到2005年的1.36cm,2008年进一步降低到1.05cm[24]。
从生存率来看,1993~1995年开展筛查前韩国甲状腺癌患者的5年相对生存率为94.5%,开展筛查后5年内(也就是2001~2005年)提升至98.4%,从2006年开始已达到100%(图2)[25]。
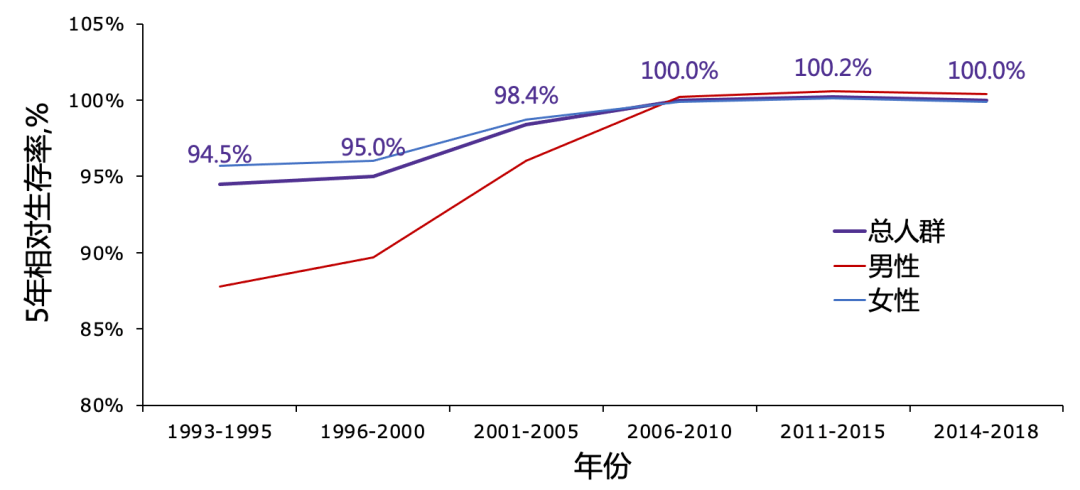
图2 1983~2018年韩国甲状腺癌5年相对生存率变化趋势(来源:韩国中央癌症登记)
◊ 英国:疗效提升进程落后于欧美主流
1985~1989年间,英国甲状腺癌的5年相对生存率为男性64%、女性75%,低于同时间段欧洲的平均水平(男性72%、女性80%)[26]。1995~1999年间,英国甲状腺癌的5年相对生存率为77.6%[27],与欧洲平均水平的差距缩小了,与同时期黑色素瘤、淋巴瘤、乳腺癌的生存率水平相当,低于睾丸癌。
对此,英国学者反思原因在于对甲状腺癌治疗不足和不规范[28],例如对1988年在英国伯明翰伊丽莎白女王医院就诊的205例DTC病例进行回顾性分析[29]发现:12%~20%的患者没有得到充分手术、放射性碘治疗和TSH抑制治疗,14.6%没有监测血清Tg水平。
2002年,英国甲状腺学会发布指南以提高治疗的彻底性和规范性,到2000-2007年英国甲状腺癌生存率已提高到男性77%、女性83%(图3)[30]。
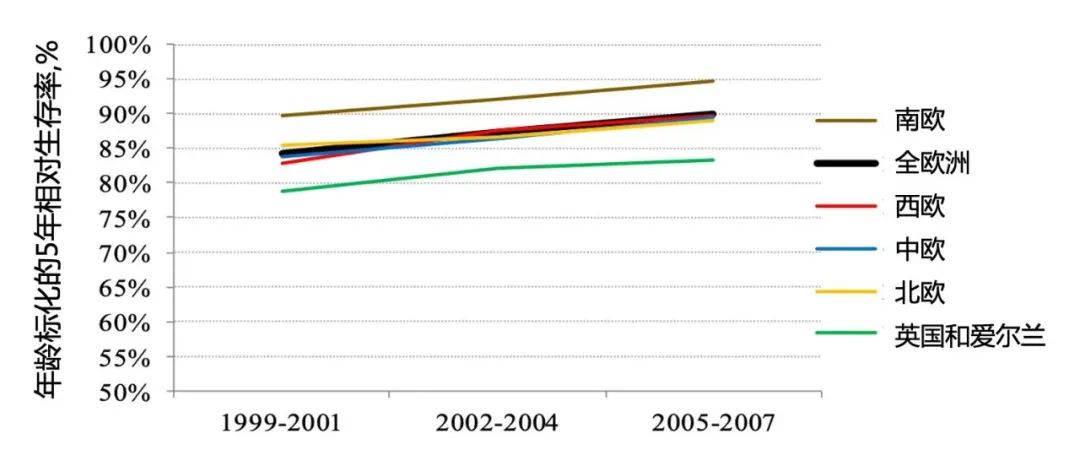
图3 欧洲不同时间段、不同地区成人甲状腺癌的5年相对生存率变化趋势(来源:EUROCARE-5数据库)
◊ 中国:尚不可对标欧美,欠发达地区规范诊疗任重道远
2003~2005年我国甲状腺癌的5年相对生存率仅为67.5%[31],与美国1940~1949年水平相当;但经过短短十年,到2012~2015年,我国甲状腺癌生存率已跃升至83.4%,但仍与美国有14%的差距[32]。
另外,我国的医疗卫生发展存在明显的区域不平衡性,医疗资源相对发达的地区如上海市浦东区,截至2015年甲状腺癌的5年相对生存率已达到100%[33],同时期福建省厦门市为94.2%[34]。
而医疗资源欠发达地区如甘肃省,2018年甲状腺癌死亡率仍高于全国平均水平(0.5/10万 vs. 0.37/10万)[35],由此可见在甲状腺癌管理上,我国医疗资源欠发达地区与发达地区仍存在较大差异。
♦ 对各国历史数据的思考
随着诊疗技术和规范性的提高,甲状腺癌的治疗效果有了长足进步,但这并不是甲状腺癌与生俱来的结局,不能据此否定甲状腺癌积极和规范诊疗的意义。
迄今为止,由于我们对甲状腺癌的认识和精准区分亚型的能力还十分有限,加上世界各国和各地区的诊疗效果演进的历程各不相同,对经验教训的总结也不同。美国疗效提高更早接近极限,认为可以更少付出代价,转而相对保守;韩国从积极诊疗中获益更大,态度依然相对积极;英国诊疗效果落后于欧美主流,与中国相似;中国则地区、城乡差异巨大,认识更难统一。
因此,真实世界和指南都不尽相同,存在不少困惑。面对甲状腺癌 “过度诊疗” 这一争议,积累中国数据、进行更深入和科学的研究是解决困惑的根本路径。我们已经和正在推行的专科化和专科医生培养是现实选择,而规范化诊疗与因地制宜,逐步缩小城乡、地区、医院差别也势在必行。
参考文献:
全球范围内甲状腺癌患病人数不断攀升,年发病数已从2000年的12.3万[1]上升至2020年的58.6万[2],20年间增长了4.77倍,成为了“流行病”。相比之下甲状腺癌死亡率则维持在较低水平[3]。乳头状癌(PTC)是甲状腺癌最常见的病理类型[4],全球范围内甲状腺癌发病率增加主要归因于PTC增加[5]。以1974~2013年间美国统计数据为例,PTC及微小癌(肿瘤直径≤1.0cm)增速最高[6]。
高发病率背景下相对较低的死亡率,以及疾病谱向PTC和微小癌转变,引发了学术界对甲状腺癌 “过度诊疗” 的争议,也为临床医生带来一些困惑。那么,应该如何理解不同国家指南以及真实世界诊疗上的差异呢?本文特邀华中科技大学附属协和医院黄韬教授展开细致解读,现将内容整理如下。

黄韬教授,华中科技大学附属协和医院
博士研究生导师、华中科技大学附属协和医院外科教研室主任、华中科技大学附属协和医院乳腺甲状腺外科主任、中国医促会普通外科学分会主任委员、中国医师协会外科医师分会甲状腺外科医师委员会副主委、中国研究型医院学会甲状腺疾病专业委员会副主委、中国研究型医院学会甲状腺疾病专业委员会临床研究学组组长、中华医学会外科学分会甲状腺及代谢外科学组委员、中华医学会肿瘤学分会甲状腺肿瘤专业委员会委员、中国抗癌协会甲状腺癌专业委员会常委、中国抗癌协会乳腺癌专业委员会委员、湖北省临床肿瘤学会甲状腺癌专委会主委、湖北省抗癌协会甲状腺癌专委员会副主委
♦ 甲状腺癌管理:美国指南已出现诊疗降级趋势,其他国家仍相对积极
◊ 甲状腺微小癌的诊断:欧美趋于保守,中日韩英更积极
2015年美国ATA指南推荐:超声高度怀疑恶性的结节行细针穿刺活检(FNA)的指征是肿瘤直径≥1.0cm,较之前阈值有所提高,有诊断降级倾向 [7,8]。
与美国一致,欧洲指南[9]也不建议对≤1.0cm的结节行FNA。这实际可能限制和减少了对微小癌的诊断,是否意味着即使超声高度怀疑恶性,微小癌也不推荐穿刺评估,不需要诊断?中国[10]、日本[11]、韩国[12]则将FNA阈值定为0.5cm,英国[13]建议若临床怀疑淋巴结转移即使结节≤1.0cm也应行FNA,对微小癌诊断更为积极。

表1 各国指南对≤1cm甲状腺结节FNA的推荐意见
注:ATA=美国甲状腺学会,ESMO=欧洲肿瘤内科学会,CATO=抗癌协会甲状腺癌专业委员会,KTA=韩国甲状腺学会,JTA=日本甲状腺学会
◊ 甲状腺微小癌的管理:美国将主动监测加入推荐
2022年美国国立综合癌症网络(NCCN)指南[14]推荐:FNA疑诊PTC患者,若肿瘤直径≤1.0cm且颈部超声未发现淋巴结转移(cN0),可以选择主动监测(active surveillance),也可选择甲状腺腺叶切除术。但时至今日,仅有低质量循证医学证据支持主动监测用于低危PTMC,且其可操作性存疑。
◊ 1~4cm DTC的手术范围:美国趋于保守,日韩更积极
ATA指南[8]推荐:1~4cm分化型甲状腺癌(DTC)如果经临床评估未发现淋巴结转移(cN0)和腺外侵袭证据,初始手术方式可选择甲状腺全切/近全切除术或甲状腺腺叶切除术;对于低危DTC,腺叶切除可能就已足够。
韩国指南[12]则认为1~4cm DTC无淋巴结转移和腺外侵袭的情况非常少见,全切对于此类患者几乎是必须的;而且韩国外科医生的手术量普遍较高,手术并发症发生率低于其他国家;综上所述,建议在全/近全切和腺叶切除中灵活选择[12]。日本指南[15]则将行甲状腺全切术的肿瘤界值确定在2cm。
综上所述,在 “过度诊疗” 背景下,美国指南对甲状腺癌诊断与治疗的推荐已趋于保守,而英国、韩国、中国则相对积极,是什么原因造成了这种差异?回顾各国甲状腺癌治疗效果的演变历程,或许能找到答案。
♦ 以史为鉴,强调甲状腺癌“过度诊疗”为时尚早
◊ 美国:疗效更早接近极限,治疗降级后隐忧初现
1940~1949年间,美国甲状腺癌的5年相对生存率仅为64%[16],受限于有限的检测手段,此时期接受外科手术的患者普遍分期晚、肿瘤较大或已出现广泛颈部转移、远处转移;同时手术范围通常较为保守,在切除肉眼可见的癌灶同时尽可能保留剩余甲状腺。
1950年后,人们逐渐认识到不彻底的手术将增加肿瘤残留风险,增加复发和死亡率,故而开始引入甲状腺全切术、甲状腺腺叶切除术、颈部淋巴结清扫等术式。1965~1969年,美国甲状腺癌5年生存率提升至84%。
1970年开始,Mazzaferri等众多学者开始探索术后放射性碘治疗、TSH抑制治疗在改善DTC预后方面的价值[17]。分析1985~1995年美国国家癌症数据库(NCDB)[18]中5.3万例病例资料发现,DTC患者接受标准甲状腺手术(甲状腺全/近全切除术或腺叶切除术)的比例已近80%,全切术后放射性碘治疗比例达到38.3%,此时PTC、FTC的5年相对生存率已分别达到96%、91%。可见随着诊疗技术和规范性的提高,美国甲状腺癌疗效更早接近极限。
诊疗降级是否会影响甲状腺癌预后?分析2000-2017年美国加州6.9万甲状腺癌登记数据[19]发现,2014年后PTC、未分化癌、局部扩散及转移癌、大癌的年死亡率均呈增长态势(图1)。这是否是2009年ATA指南的5年后效应?2015年ATA指南又会对甲状腺癌的生存率和死亡率产生什么影响?仍需长时间观察。

图1 2001~2016年甲状腺癌年死亡率变化趋势(来源:美国加州肿瘤登记数据库)
◊ 韩国:从积极诊疗中获益更大
1999年,韩国政府发起一项全民免费肿瘤筛查项目,由于颈部超声价格低廉,很多医院将甲状腺癌超声筛查加入筛查套餐[20]。这一举措导致2000年以后韩国确诊甲状腺癌人数迅速上升,2011年相比1993年发病率升高的15倍,引发对“过度诊断”争议。但韩国筛查真的没有获益吗?
回顾韩国流行病学数据发现:从开展筛查项目5年后(也就是2005年)开始,甲状腺癌特异性死亡率开始下降[21];2003~2015年死亡率的APC约下降4.3%[22]。
从肿瘤分期来看,筛查不仅检出了更多微小癌,也提高了大癌、淋巴结转移和转移癌的检出率[23]。确诊时肿瘤直径从1999年的2.15cm降低到2005年的1.36cm,2008年进一步降低到1.05cm[24]。
从生存率来看,1993~1995年开展筛查前韩国甲状腺癌患者的5年相对生存率为94.5%,开展筛查后5年内(也就是2001~2005年)提升至98.4%,从2006年开始已达到100%(图2)[25]。

图2 1983~2018年韩国甲状腺癌5年相对生存率变化趋势(来源:韩国中央癌症登记)
◊ 英国:疗效提升进程落后于欧美主流
1985~1989年间,英国甲状腺癌的5年相对生存率为男性64%、女性75%,低于同时间段欧洲的平均水平(男性72%、女性80%)[26]。1995~1999年间,英国甲状腺癌的5年相对生存率为77.6%[27],与欧洲平均水平的差距缩小了,与同时期黑色素瘤、淋巴瘤、乳腺癌的生存率水平相当,低于睾丸癌。
对此,英国学者反思原因在于对甲状腺癌治疗不足和不规范[28],例如对1988年在英国伯明翰伊丽莎白女王医院就诊的205例DTC病例进行回顾性分析[29]发现:12%~20%的患者没有得到充分手术、放射性碘治疗和TSH抑制治疗,14.6%没有监测血清Tg水平。
2002年,英国甲状腺学会发布指南以提高治疗的彻底性和规范性,到2000-2007年英国甲状腺癌生存率已提高到男性77%、女性83%(图3)[30]。

图3 欧洲不同时间段、不同地区成人甲状腺癌的5年相对生存率变化趋势(来源:EUROCARE-5数据库)
◊ 中国:尚不可对标欧美,欠发达地区规范诊疗任重道远
2003~2005年我国甲状腺癌的5年相对生存率仅为67.5%[31],与美国1940~1949年水平相当;但经过短短十年,到2012~2015年,我国甲状腺癌生存率已跃升至83.4%,但仍与美国有14%的差距[32]。
另外,我国的医疗卫生发展存在明显的区域不平衡性,医疗资源相对发达的地区如上海市浦东区,截至2015年甲状腺癌的5年相对生存率已达到100%[33],同时期福建省厦门市为94.2%[34]。
而医疗资源欠发达地区如甘肃省,2018年甲状腺癌死亡率仍高于全国平均水平(0.5/10万 vs. 0.37/10万)[35],由此可见在甲状腺癌管理上,我国医疗资源欠发达地区与发达地区仍存在较大差异。
♦ 对各国历史数据的思考
随着诊疗技术和规范性的提高,甲状腺癌的治疗效果有了长足进步,但这并不是甲状腺癌与生俱来的结局,不能据此否定甲状腺癌积极和规范诊疗的意义。
迄今为止,由于我们对甲状腺癌的认识和精准区分亚型的能力还十分有限,加上世界各国和各地区的诊疗效果演进的历程各不相同,对经验教训的总结也不同。美国疗效提高更早接近极限,认为可以更少付出代价,转而相对保守;韩国从积极诊疗中获益更大,态度依然相对积极;英国诊疗效果落后于欧美主流,与中国相似;中国则地区、城乡差异巨大,认识更难统一。
因此,真实世界和指南都不尽相同,存在不少困惑。面对甲状腺癌 “过度诊疗” 这一争议,积累中国数据、进行更深入和科学的研究是解决困惑的根本路径。我们已经和正在推行的专科化和专科医生培养是现实选择,而规范化诊疗与因地制宜,逐步缩小城乡、地区、医院差别也势在必行。
参考文献: