2023年8月7日,美国埃默里大学医学院 Erik C. B. Johnson 团队在 Nature Medicine 发表了一篇题为 Cerebrospinal fluid proteomics define the natural history of autosomal dominant Alzheimer’s disease 的论文,利用蛋白质组学方法,研究了常染色体显性阿尔茨海默病(ADAD)患者脑脊液60年的变化,探索了其病理过程的演变以及与之发展相关的生物标志物。

AD 是一种 “毁灭性” 的神经退行性疾病,在老龄化社会中患病率不断增加。目前,我们没有客观的、易于评估的AD诊断标志物,也没有很好的治疗选择。
AD 的病理变化在认知症状出现前许多年就已形成。两种病理过程——β-淀粉样蛋白(Aβ)肽聚集成斑块以及微管蛋白 tau 聚集成神经原纤维缠结(NFT),是该疾病的标志。其他病理性大脑过程也被认为是Aβ斑块和 NFT 病理的关键调节因子,但这些其他病理过程是如何随病程演变的目前尚不清楚。
研究对象为具有三种基因(APP、PSEN1、PSEN2)ADAD突变携带风险的个体,包括突变携带者和来自同一家庭的非携带者。这些参与者在DIAN(显性遗传阿尔茨海默氏症研究网络)观察性研究中接受评估,每1到3年进行一次随访。评估内容包括收集体液(脑脊液、血液)、临床测试(临床痴呆评分)、神经心理学测试和成像模态(磁共振成像、PIB-PET和18F-FDG)。
研究展示了在 ADAD 脑脊液中进行的蛋白质组学测量:使用定向蛋白质组学方法,通过选择反应监测质谱法(SRM-MS)测量了 ADAD 突变携带者和非携带者的脑脊髓液中的59种蛋白质,并将这些测量结果与脑蛋白的共表达模块进行关联分析,所得结果可用于描述AD病理学在长达60年的时间尺度上的演变特征。
研究发现,与Aβ斑块相关的 SMOC1 和 SPON1 蛋白在 AD 临床症状发作前近30年就在脑脊髓液中升高,随后是突触蛋白、代谢蛋白、轴突蛋白、炎症蛋白的变化,最后是神经分泌蛋白的下降。这些蛋白质的组合能够在症状出现之前,就很好地将常染色体显性 AD 突变携带者与非携带者区分开来,甚至表现要比Aβ和tau的测量结果更好。
这些结果强调了 AD 病理生理学的多方面景观及其时间演变,这对于开发 AD 的精准治疗干预和超越Aβ和tau的生物标志物而言具有重要意义。
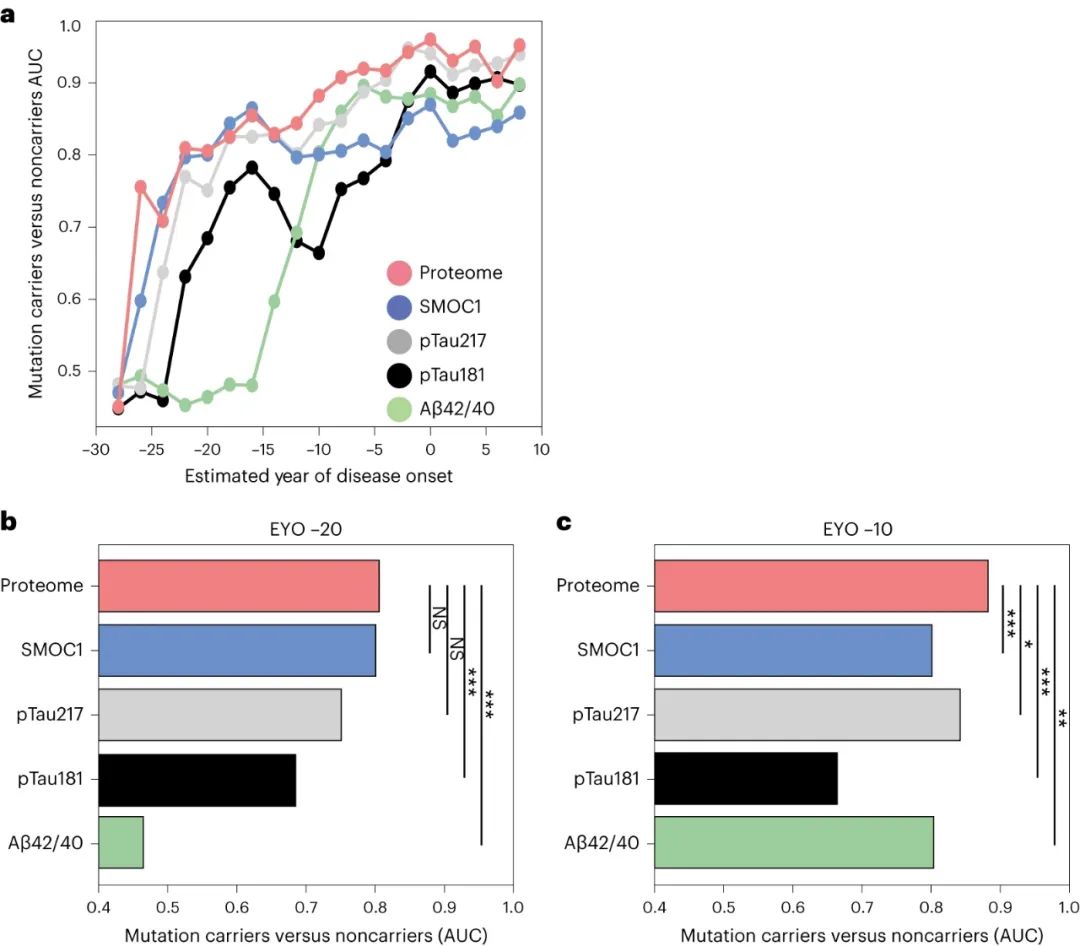
通过深入分析 AD 脑脊液蛋白质组学数据,研究揭示了阿尔茨海默病病理的复杂性和演变过程,提出了针对不同阶段的治疗干预的可能性。
研究提出,在阿尔茨海默病的治疗干预方面,至少有三个关键时期:Aβ斑块形成前30年、轴突和白质完整性问题开始前19年,以及炎症反应强烈开始前6年,这些时期可能是进行AD治疗干预的最佳时机。此外,研究还强调了蛋白质组学在AD早期诊断和分类方面的潜力。
尽管该研究在 ADAD 患者中提供了有关病理变化的重要见解,但它的样本量相对较小,主要关注 ADAD 这一特定遗传类型的患者。未来,该领域的研究可以考虑扩大样本规模,探索与其他类型 AD(如散发性阿尔茨海默病)之间的差异。此外,尽管蛋白质组学提供了深入了解 AD 疾病的方法,但蛋白质与基因、代谢和其他分子之间的相互作用仍然复杂,我们需要更多的多组学、综合性研究。
- 本文借助了ChatGPT进行辅助解读,研究详情请参见论文原文。解读若有错漏之处,欢迎大家指正 -








