2023年5月16日,中国医学科学院血液病医院(中国医学科学院血液学研究所)程涛、朱平、周家喜、王洪课题组,联合西湖大学郭天南、南开大学沈中阳及天津大学王西墨,共同在Immunity在线发表了题为 Multi-omics blood atlas reveals unique features of immune and platelet responses to SARS-CoV-2 Omicron breakthrough infection 的研究论文。该研究应用蛋白质组、代谢组和免疫组库等多组学方法,分析并揭示了Omicron感染者的血液生态系统。

新冠大流行是人类历史上最为严重的大流行病之一。截至2022年10月,已有6亿多人感染新冠病毒,累计死亡人数超600万。在众多新冠病毒变体中,Omicron最受关注。
相比原始新冠毒株,Omicron毒株毒力较低,但感染力强。因此,Omicron对于免疫缺陷或需要免疫抑制治疗的潜在疾病人群而言仍然是一种危及生命的感染。然而,此前与Omicron相关的不同疾病阶段和严重程度的分子及细胞变化动态尚未完全阐明。
而且,据报道,很大一部分的Omicron感染者会出现 “复阳” 现象(病毒RNA检测呈阳性),这种 “复阳” 是一种特殊的临床现象,涉及可检测到的病毒RNA的复发,而不是由于再次感染或假阳性/假阴性检测所引起。
“复阳” 背后潜在的分子机制及其对Omicron传播性增强的潜在影响很大程度上仍未可知,目前也没有有效的策略来预测患者的复阳风险。因此,应用血液生态系统理念剖析奥密克戎病毒感染,对其诊疗与防控具有重要意义。
该研究使用多组学因子分析(MOFA),对Omicron感染患者的1000多份血细胞/血浆样本的临床表型、转录组、蛋白质组、代谢组和免疫组库进行了系统分析。利用无偏差的因子分析多组学数据,剖析了宿主在多个疾病阶段的反应动态,揭示了血液中的分子和细胞景观,对Omicron突破性感染者的血液生态系统进行了不同疾病阶段的研究。
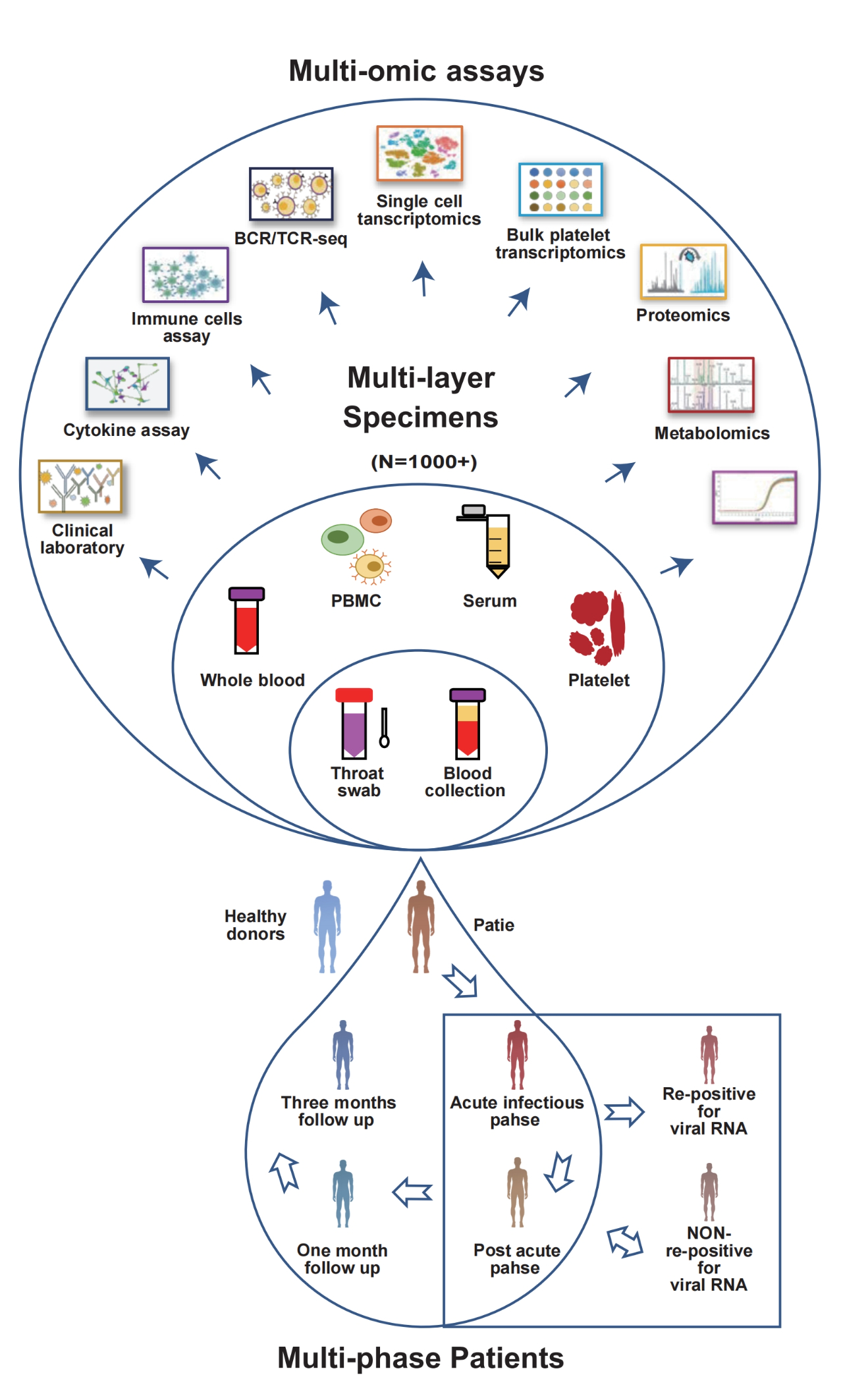
图1 SARS-CoV-2奥密克戎患者血液生态系统多组学研究设计
具体而言,研究人员在Omicron感染者中检测到增强的干扰素介导的血小板抗病毒特征,并且血小板优先与白细胞形成广泛的聚集,以调节免疫细胞功能。此外,“复阳” 患者的B 细胞受体克隆、抗体产生和对Omicron的中和能力都显著减少,揭示了复阳可能是由减弱的免疫反应引起的。
最后,研究人员整合临床指标、血浆蛋白质组和代谢组,开发了一组机器学习模型,利用该模型所发现的与宿主免疫反应密切相关一组血浆分子生物标志物,可以准确预测Omicron患者复阳的概率。
该研究进一步展示了抗体或血浆疗法在预防和治疗Omicron复阳患者方面的潜力,可能会激发研究系统性疾病和新发公卫问题的范式转变。
♦ Omicron感染者的血浆蛋白质组和代谢组研究
研究者对Omicron患者和健康对照进行了血浆蛋白质组学和代谢组学分析,定量了546种代谢物和803种蛋白质。然后,使用代谢和蛋白质组学数据探索了健康对照、急性感染期、康复期之间的差异。在血浆代谢组和蛋白质组内,共有447种代谢物和476种蛋白质差异表达(B-H adjusted p值 < 0.05)(图2A和2C)。血浆蛋白质组和代谢组显示Omicron感染后出现明显的血小板失调,研究揭示血小板在奥密克戎感染期间起关键作用。
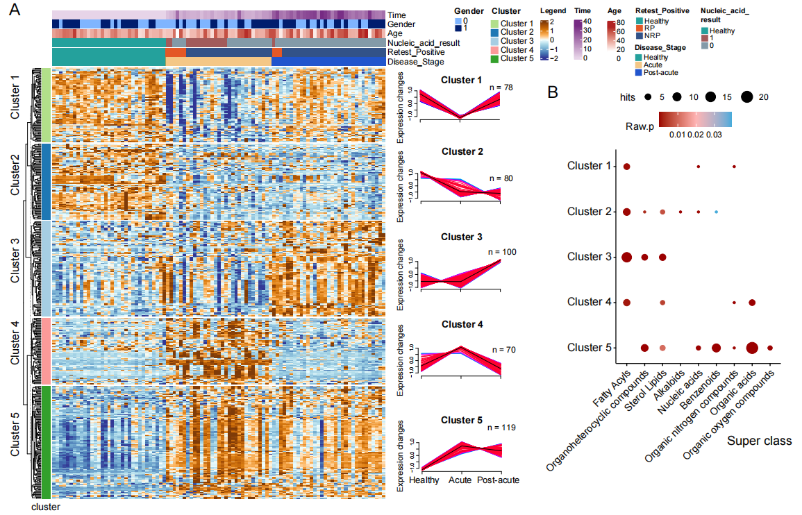
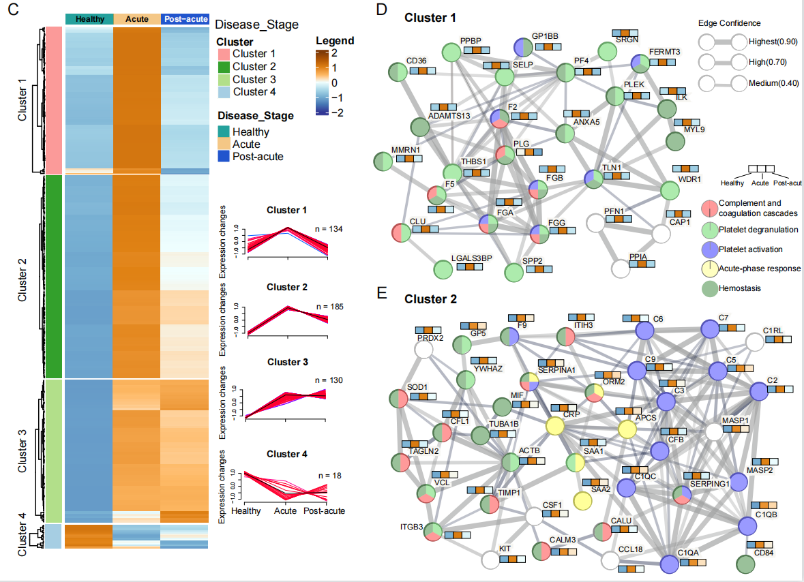
图2 血浆蛋白质组和代谢组揭示奥密克戎患者明显的血小板相关失调
通过UMAP分析,差异表达代谢物DEMs和差异表达蛋白DEPs可以较为准确地对不同疾病阶段进行聚类,这些DEMs和DEPs可能成为监测奥密克戎疾病过程的候选分子生物标志物。DEMs和DEPs的联合分析再次确定了血小板活化,补体和凝血级联以及不饱和脂肪酸等的生物合成在Omicron感染后不同时期发生了较为显著的变化。
在制定针对快速传播的奥密克戎的策略方面,复阳患者是其中一个待解决的问题,考虑到奥密克戎的复阳率很高,需要能够预测可能出现阳性病毒RNA的患者。为此,研究人员整合临床指标、血浆蛋白质组和代谢组,开发了机器学习模型,该模型可有效预测患者复阳性的可能性(图3)。
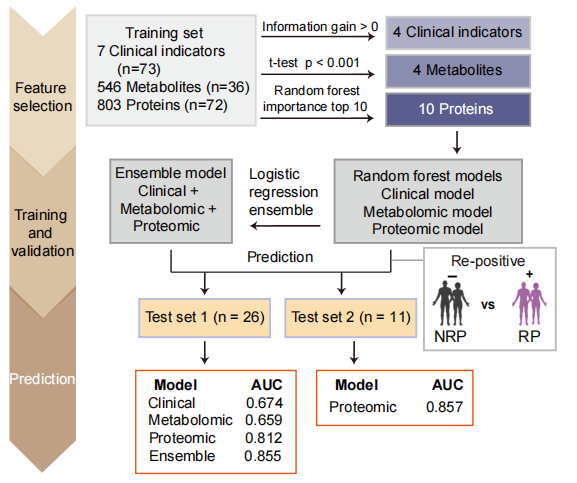
图3 机器学习模型构建流程和结果
该研究也存在一定的局限性,如Omicron的突破性感染可能受到疫苗接种等因素的影响,因此,需要独立的高质量标本队列来进一步研究该模型的有效性。
⇒ 生态系统(ecosystem),是描述一个确定环境或空间中所有成分及相互作用的概念,这一概念多用在地球和海洋生态领域中,现在也被用于肿瘤和肠道微生物等生命健康领域。
原文链接:https://doi.org/10.1016/j.immuni.2023.05.007
2023年5月16日,中国医学科学院血液病医院(中国医学科学院血液学研究所)程涛、朱平、周家喜、王洪课题组,联合西湖大学郭天南、南开大学沈中阳及天津大学王西墨,共同在Immunity在线发表了题为 Multi-omics blood atlas reveals unique features of immune and platelet responses to SARS-CoV-2 Omicron breakthrough infection 的研究论文。该研究应用蛋白质组、代谢组和免疫组库等多组学方法,分析并揭示了Omicron感染者的血液生态系统。

新冠大流行是人类历史上最为严重的大流行病之一。截至2022年10月,已有6亿多人感染新冠病毒,累计死亡人数超600万。在众多新冠病毒变体中,Omicron最受关注。
相比原始新冠毒株,Omicron毒株毒力较低,但感染力强。因此,Omicron对于免疫缺陷或需要免疫抑制治疗的潜在疾病人群而言仍然是一种危及生命的感染。然而,此前与Omicron相关的不同疾病阶段和严重程度的分子及细胞变化动态尚未完全阐明。
而且,据报道,很大一部分的Omicron感染者会出现 “复阳” 现象(病毒RNA检测呈阳性),这种 “复阳” 是一种特殊的临床现象,涉及可检测到的病毒RNA的复发,而不是由于再次感染或假阳性/假阴性检测所引起。
“复阳” 背后潜在的分子机制及其对Omicron传播性增强的潜在影响很大程度上仍未可知,目前也没有有效的策略来预测患者的复阳风险。因此,应用血液生态系统理念剖析奥密克戎病毒感染,对其诊疗与防控具有重要意义。
该研究使用多组学因子分析(MOFA),对Omicron感染患者的1000多份血细胞/血浆样本的临床表型、转录组、蛋白质组、代谢组和免疫组库进行了系统分析。利用无偏差的因子分析多组学数据,剖析了宿主在多个疾病阶段的反应动态,揭示了血液中的分子和细胞景观,对Omicron突破性感染者的血液生态系统进行了不同疾病阶段的研究。

图1 SARS-CoV-2奥密克戎患者血液生态系统多组学研究设计
具体而言,研究人员在Omicron感染者中检测到增强的干扰素介导的血小板抗病毒特征,并且血小板优先与白细胞形成广泛的聚集,以调节免疫细胞功能。此外,“复阳” 患者的B 细胞受体克隆、抗体产生和对Omicron的中和能力都显著减少,揭示了复阳可能是由减弱的免疫反应引起的。
最后,研究人员整合临床指标、血浆蛋白质组和代谢组,开发了一组机器学习模型,利用该模型所发现的与宿主免疫反应密切相关一组血浆分子生物标志物,可以准确预测Omicron患者复阳的概率。
该研究进一步展示了抗体或血浆疗法在预防和治疗Omicron复阳患者方面的潜力,可能会激发研究系统性疾病和新发公卫问题的范式转变。
♦ Omicron感染者的血浆蛋白质组和代谢组研究
研究者对Omicron患者和健康对照进行了血浆蛋白质组学和代谢组学分析,定量了546种代谢物和803种蛋白质。然后,使用代谢和蛋白质组学数据探索了健康对照、急性感染期、康复期之间的差异。在血浆代谢组和蛋白质组内,共有447种代谢物和476种蛋白质差异表达(B-H adjusted p值 < 0.05)(图2A和2C)。血浆蛋白质组和代谢组显示Omicron感染后出现明显的血小板失调,研究揭示血小板在奥密克戎感染期间起关键作用。


图2 血浆蛋白质组和代谢组揭示奥密克戎患者明显的血小板相关失调
通过UMAP分析,差异表达代谢物DEMs和差异表达蛋白DEPs可以较为准确地对不同疾病阶段进行聚类,这些DEMs和DEPs可能成为监测奥密克戎疾病过程的候选分子生物标志物。DEMs和DEPs的联合分析再次确定了血小板活化,补体和凝血级联以及不饱和脂肪酸等的生物合成在Omicron感染后不同时期发生了较为显著的变化。
在制定针对快速传播的奥密克戎的策略方面,复阳患者是其中一个待解决的问题,考虑到奥密克戎的复阳率很高,需要能够预测可能出现阳性病毒RNA的患者。为此,研究人员整合临床指标、血浆蛋白质组和代谢组,开发了机器学习模型,该模型可有效预测患者复阳性的可能性(图3)。

图3 机器学习模型构建流程和结果
该研究也存在一定的局限性,如Omicron的突破性感染可能受到疫苗接种等因素的影响,因此,需要独立的高质量标本队列来进一步研究该模型的有效性。
⇒ 生态系统(ecosystem),是描述一个确定环境或空间中所有成分及相互作用的概念,这一概念多用在地球和海洋生态领域中,现在也被用于肿瘤和肠道微生物等生命健康领域。
原文链接:https://doi.org/10.1016/j.immuni.2023.05.007









