胶质母细胞瘤(glioblastoma,GBM)是成人中最常见和致命的原发性脑肿瘤之一。然而,患者在治疗后的复发问题仍然没有得到有效解决。以往虽然通过基因组学的研究揭示了肿瘤在治疗后的演变,但这些平台未能找到能够解释复发性疾病普遍伴随的治疗抵抗的一致性演变轨迹。
为了解决这些问题,有研究人员采用了蛋白质组学+基因组学+转录组学的多组学方法,更全面地揭示了GBM在治疗后的演变。

图1 论文截图
2024年1月11日,韩国国立癌症研究中心 Jong Bae Park 团队、美国迈阿密大学医学院 Antonio Iavarone 团队、韩国三星医疗中心 Do-Hyun Nam 团队、法国巴黎神经科学研究所 Marc Sanson 团队等合作在 Cancer Cell 发表了蛋白组学新文章:Integrated proteogenomic characterization of glioblastoma evolution。
文章揭示了在治疗过程中,复发性胶质母细胞瘤(GBM)发生神经细胞状态的演变,伴随着WNT/PCP信号通路的激活、DAMM1的显著贡献以及BRAF活性的主导,强调神经元活动及突触形成在复发GBM中的关键作用。
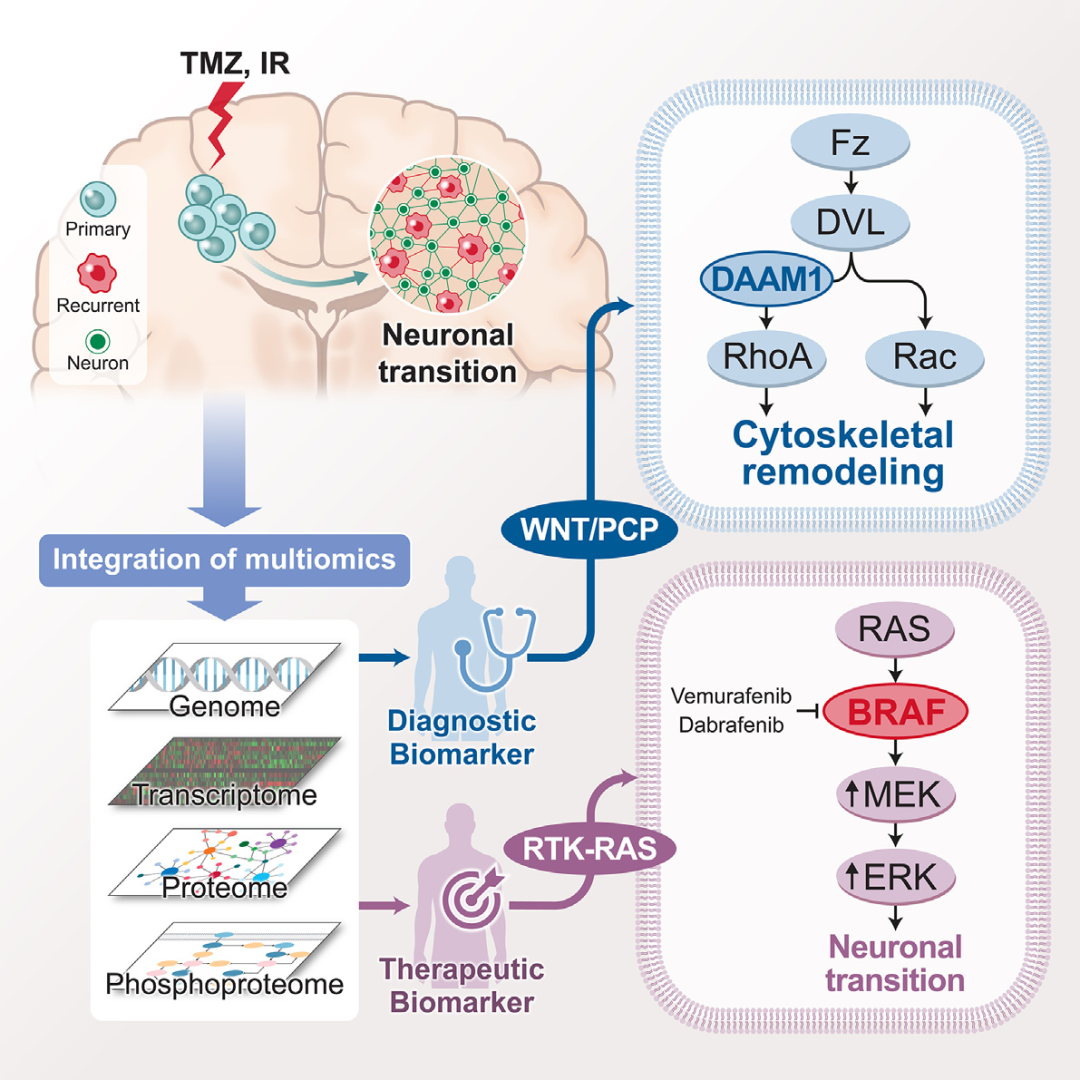
图2 图文摘要
结论1:
胶质母细胞瘤的纵向分子轨迹
研究人员从5个不同机构收集了123例纵向收集的GBM样本,并进行了全外显子测序(WES)、全转录组测序(WTS)和基于质谱的蛋白质组学分析。其中,8例复发的肿瘤表现出高度突变性,与错配修复(MMR)编码基因的遗传变异以及TMZ诱导的突变特征相关。
IDH1突变在演变过程中表现出一致稳定,而EGFR的染色体扩增、CDKN2A的缺失以及PTEN、ATRX、TP53的体细胞突变在未治疗和复发肿瘤中高度一致。然而,复发肿瘤中CDK6、MDM4和CCND2的染色体扩增等基因的遗传变异频率较低,这些基因主要参与细胞周期和增殖动力学,这表明复发的GBM可能不再通过传统的增强细胞周期进程和增殖的机制维持。
通过整合mRNA表达和CNV数据,研究人员发现主要的GBM驱动变异在原发和复发肿瘤中维持一致。然而,在细胞周期、有丝分裂和DNA修复活动中参与的一些基因(ERCC2、HUS1、PDGFA等)在原发GBM中显著富集,而在复发肿瘤中显著减少。相反,复发GBM富集了与神经分化有关的基因(SGK2、LIN7B、STX1A等)。
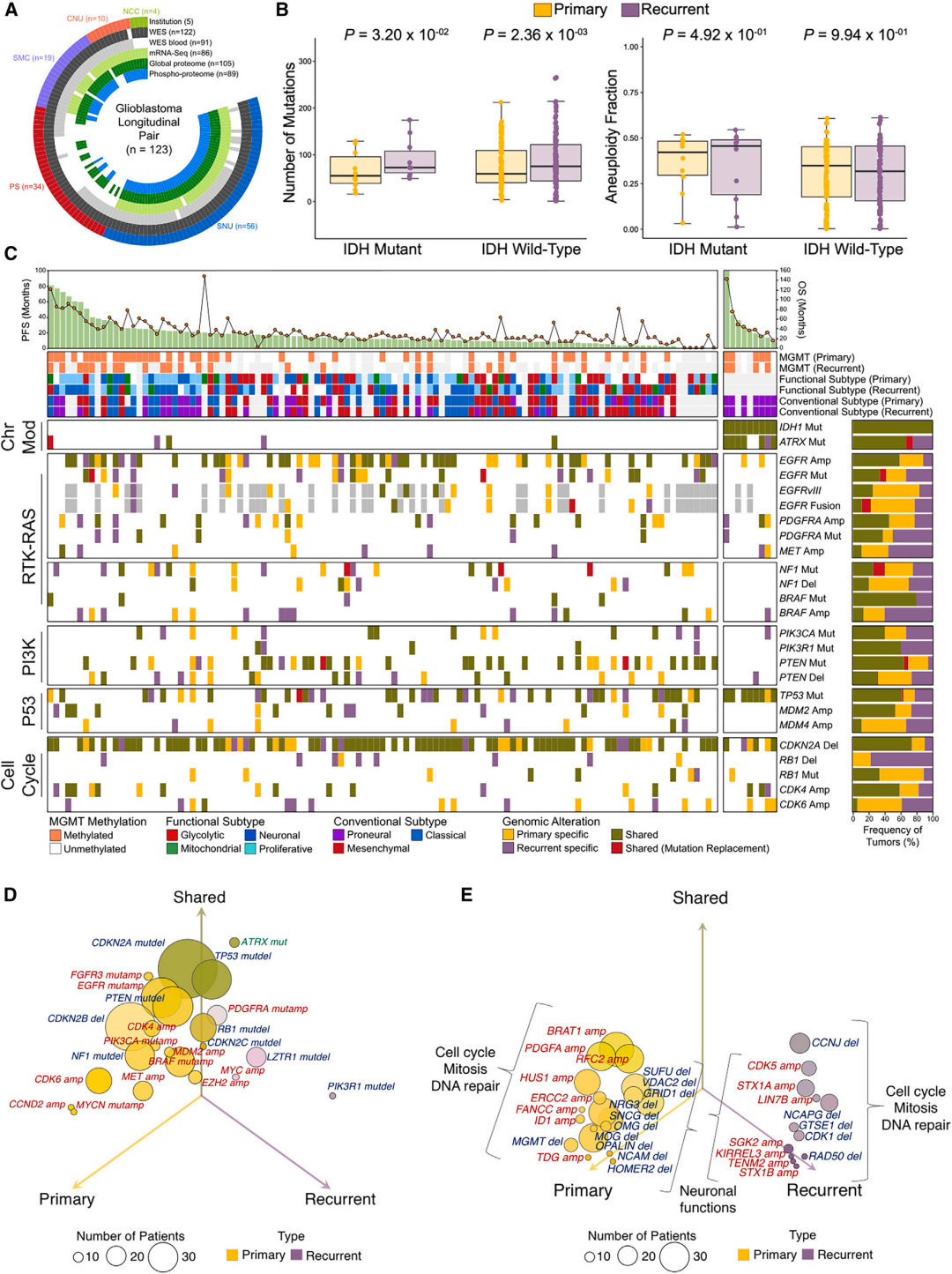
图3 胶质母细胞瘤的纵向分子轨迹
结论2:
EGFR基因改变对复发性脑胶质瘤下游信号传导的影响
研究人员发现,与初发性肿瘤相比,复发性肿瘤中主要富集了FGFR2/3、NTRK2/3和BRAF蛋白,而EGFR、CDK4和CDK6蛋白在初发性肿瘤中丰度增加。这些肿瘤蛋白的积累与基因拷贝数和mRNA水平的相应变化无关,提示这些蛋白激酶在GBM演变中可能受到转录后调控。
EGFR基因改变是GBM发生的主要因素之一,但其在推动GBM复发中的作用尚不清楚。研究分析了匹配的原发-复发性GBM样本中EGFR基因改变的动态,发现患者可分为三组,其中一组在原发性和复发性肿瘤中均表现出EGFR改变;而另外两组中,EGFR改变在复发性肿瘤中要么丢失要么获得。研究还发现,EGFR改变在复发时的丢失与EGFR蛋白的降低相关。这些结果提示,在GBM的演变过程中,EGFR信号通路在很大程度上被失活,可能是由于在演变过程中EGFR蛋白的减少所致。
结论3:
纵向GBM的蛋白质基因组特征揭示了复发时神经活动的增加
通过蛋白质组学和磷酸化蛋白组学对纵向发展的脑胶质母细胞瘤(GBM)进行分析后,研究人员发现复发性GBM表现出增强的神经元活动。研究揭示了在复发性GBM中有377种蛋白和1820种磷酸化蛋白的增加,包括SNAP25、TUBB4A、NELF、DAAM1/2、STMN1和MBP等。生物通路富集分析显示,复发性肿瘤中蛋白质和磷酸化蛋白的升高与神经元结构和功能以及突触形成有关。
与此同时,原发性GBM主要富集于DNA复制、细胞增殖、丝裂原活化蛋白激酶(MAPK)调控以及细胞外基质功能和EGFR信号通路。通过整合转录组学、蛋白质组学和磷酸化蛋白组学数据,研究探讨了蛋白质调控与GBM进展中的转录控制的相关性。结果显示,在复发性GBM中,大多数蛋白与相应mRNA呈一致变化,但也存在一些蛋白与mRNA的不一致变化。
研究还探讨了遗传变异对复发时全局和磷酸化蛋白丰度的功能影响,结果表明EGFR在cis作用水平上对蛋白和磷酸化的丰度有显著下降,提示EGFR的变异在GBM的肿瘤启动中发挥作用,但在肿瘤演化中不再需要。在trans-acting水平上,复发性肿瘤中多个GBM驱动基因的遗传变异导致RAS通路、WNT通路和突触形成相关蛋白的升高。总体而言,研究结果表明复发性GBM具有独特的神经信号程序,可能受RAS和WNT信号激活的驱动,并有助于破坏初诊GBM扩张所必需的细胞增殖机制。
结论4:
综合多组学亚型分析揭示了复发性GBM中神经元GBM亚型的富集
研究人员利用基因组学、转录组学、蛋白质组学和磷酸化蛋白质组学对原发性和复发性GBM进行了综合分析。结果显示,复发性GBM在神经元亚型方面显著富集,表现出与原发性肿瘤不同的分子特征。这表明GBM在治疗过程中呈现向神经元状态演变的趋势,其调控受到遗传和后遗传分子事件的共同影响。通过对肿瘤样本的多平台分析,研究验证了复发性GBM主要表现出增强的神经元功能。
此外,对DNA修复机制关键分子的蛋白质丰度分析表明,蛋白质失活可能是GBM复发的重要机制之一。
结论5:
单细胞分析和功能实验模型揭示了复发瘤细胞中神经活动的富集
研究人员对四对原发和复发肿瘤组织标本进行了单细胞RNA测序,通过推断拷贝数变异(CNV)的方式识别了4,228个恶性细胞和12,258个非恶性细胞。
对比分析发现,在复发GBM中,少突胶质细胞和神经元的数量增加,而髓系细胞和T细胞的数量减少。就肿瘤细胞状态而言,通过基于通路的功能状态分析,发现复发GBM的演变过程中表现出增加的神经细胞状态,而干细胞/祖细胞(PPR)状态和MTC状态减少。
复发肿瘤中,神经元状态的升高与原发GBM相比显著,而包括NPC样、OPC样、AC样和MES样在内的其他胶质细胞状态的分类器没有显示出显著变化。通过计算PPR和NEU(神经元)细胞状态的活性,研究人员确认了神经功能在复发肿瘤中的全局增加。对单细胞的“简单性评分”(simplicity score)显示,神经活动是复发肿瘤的主导生物学特征。
通过使用共培养系统,研究人员验证了神经发生和突触形成在复发GBM中的关键特征。结果表明,与原发肿瘤相比,复发肿瘤细胞的数量和突触形成水平显著增加,表现为较长的神经突起。
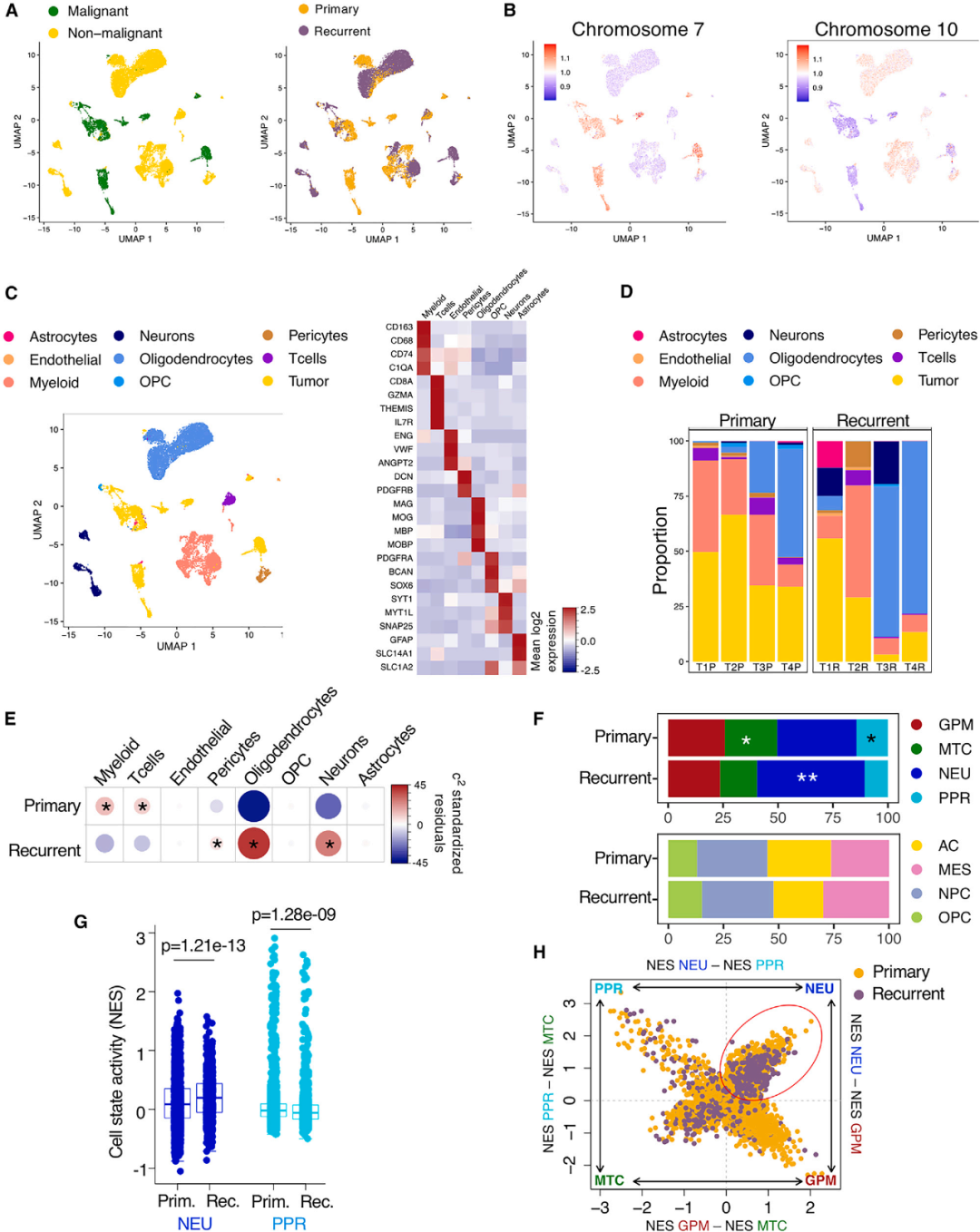
图4 单细胞分析揭示了复发性GBM肿瘤内神经元状态和肿瘤微环境中神经元和少突胶质细胞的增加
结论6:
利用体内模型系统建立复发时神经元转换的模型并对BRAF进行临床前治疗靶点测试
通过使用患者的肿瘤细胞生成PDX模型(人源性组织异种移植),研究了在治疗后发生神经元递归性胶质母细胞瘤(GBM)的演变轨迹,以及对BRAF作为治疗靶点的临床前测试。
研究人员通过在小鼠的颅内注射患者来源的肿瘤细胞后,利用磁共振成像(MRI)评估肿瘤状态,进行TMZ(替莫唑胺)或安慰剂治疗,并在多个时间点(从第7天到第41天)收集GBM组织标本进行蛋白质组学和基因组学分析。TMZ治疗显著延长了小鼠的总体存活期。
通过分析转录组学、蛋白质组学和磷酸蛋白质组学数据,研究人员鉴定了在不同时间点的独特多组学特征。在TMZ治疗的T34时间点,他们观察到了与突触结构和组织相关的神经元特征的最强烈富集。
通过建立患者特定的激酶-磷酸位点相互作用网络,研究人员发现BRAF是神经元递归性GBM中最活跃的激酶之一。进一步的实验表明,BRAF抑制剂可以阻止递归性GBM细胞的神经元特征转变,并在递归性GBM的治疗中显示出潜在的疗效。
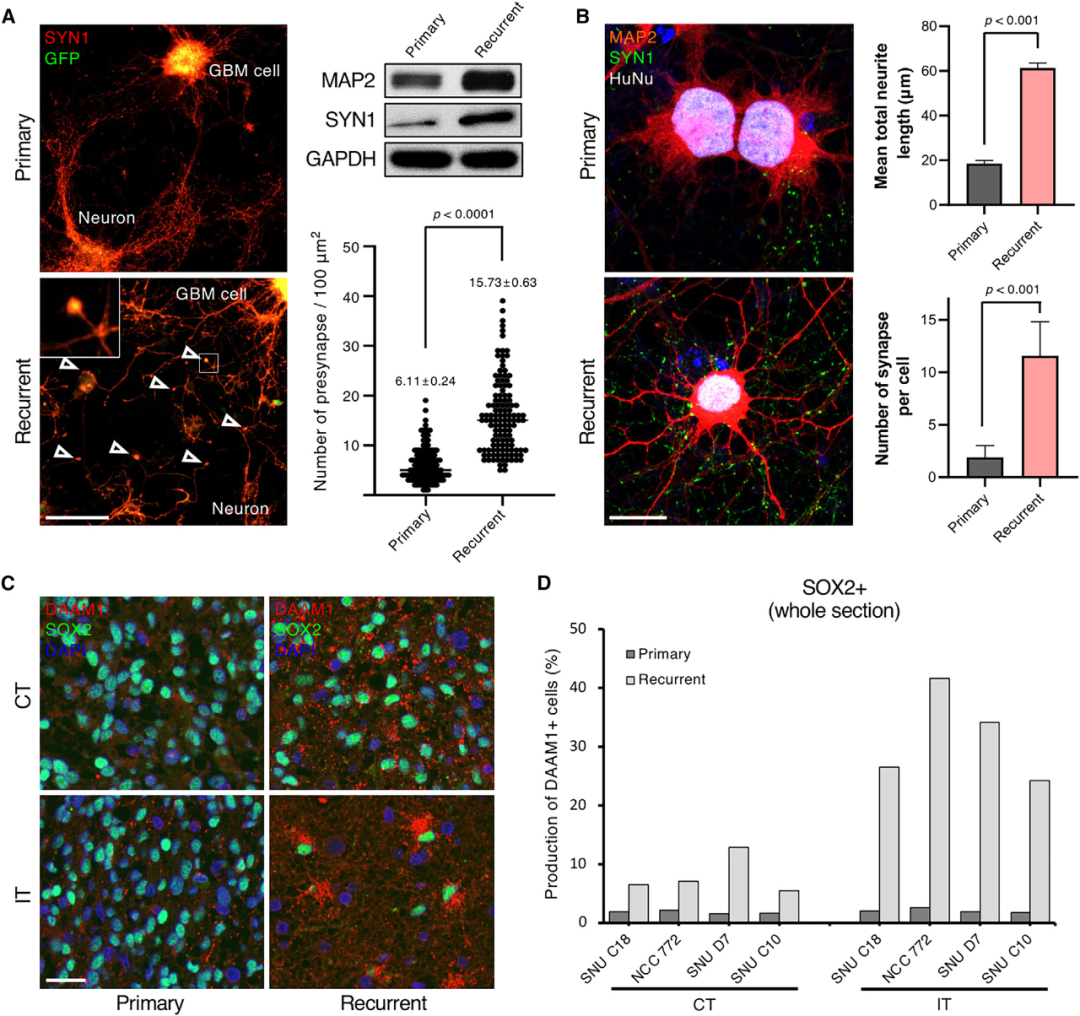
图5 复发性GBM中突触活性增强的功能验证 A:对配对的患者源性GBM细胞(原发和复发)和小鼠皮层神经元细胞进行共培养。通过免疫印迹分析测量了配对GBM细胞中MAP2和synapsin-1的表达。
总 结
总的来说,该研究通过对123例纵向收集的胶质母细胞瘤病例进行综合蛋白质组学分析,深入了解了胶质母细胞瘤演变和治疗抵抗的生物学机制,为临床干预提供了有希望的治疗策略。
文章链接:
https://www.cell.com/cancer-cell/pdf/S1535-6108(23)00443-9.pdf#%20









