♦ 空间分辨CRISPR筛选平台

图源:论文截图
2023年6月1日,慕尼黑大学Veit Hornung团队和马普所Matthias Mann团队在bioRxiv在线发表了”SPARCS, a platform for genome-scale CRISPR screening for spatial cellular phenotypes“。该文章开发了一个空间分辨CRISPR筛选(spatially resolved CRISPR screening, SPARCS)平台,利用显微镜在包含千万级别细胞的全基因组筛选文库中,物理分离不同表型细胞,实现对空间细胞表型的基因筛选。
作者首先生成了一个U2OS细胞文库表达Brunello CRISPR文库中77,441个sgRNAs,并测试了在PBS膜上对该CRISPR-U2OS细胞库进行1000个细胞核的在体显微切割,测序鉴定了其中平均549个sgRNAs,表明LMD分离细胞核用于CRISPR基因分型的可行性。随后作者构建稳定表达mCherry标记的LC3B(自噬关键蛋白)U2OS细胞,并用mTOR抑制剂Torin-1处理模拟饥饿来诱导自噬模型,通过基于深度学习的图像分类器1.0来区分Torin-1处理和未处理的mCherry-LC3 U2OS细胞,实现了< 1%的错误发现率(FDR)。
为了验证SPARCS对自噬形成相关基因分型的作用,作者构建了转染 Brunello CRISPR KO文库的120万个mCherry-LC3 U2OS细胞库 ,在Torin-1刺激下,通过SPARCS及分类器1.0分离了被分类为自噬关闭的前0.1%细胞,在这些细胞中,靶向参与自噬相关基因(比如ATG5)的sgRNA被高度富集,证明了SPARCS的有效性。为了改进分类器在识别自噬关闭细胞表现不佳的情况,作者通过改进染色和成像方案,训练了分类器2.0,并在包含千万级细胞的全基因组筛选中,进一步改进得到分类器2.1。
♦ 心脑相关性:MRI图像和基因数据的统计分析
图源:论文截图
图源:论文截图
心血管疾病与神经和精神疾病相关,而它们之间的因果联系并没有确定:可能是是由先天易感性引起的也可能是由身体状况引起的压力引起的。
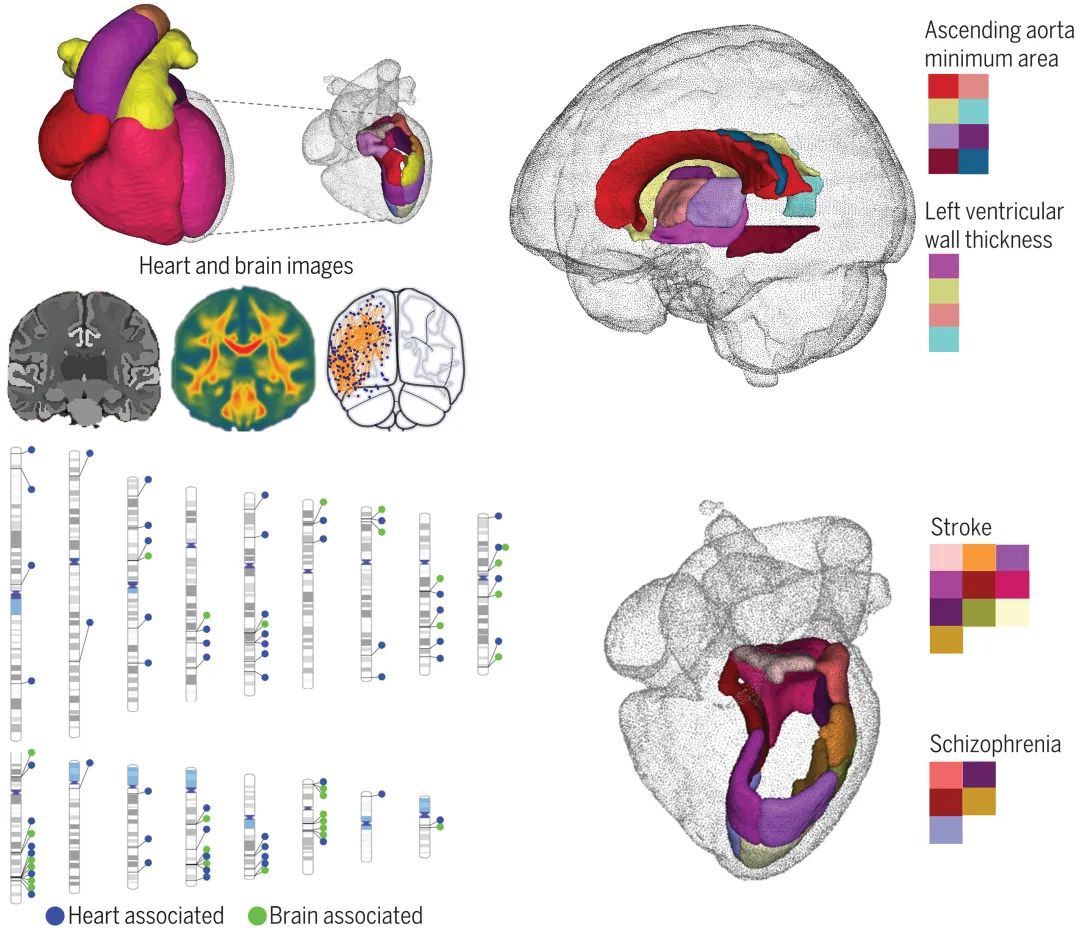
来自北卡罗来纳州教堂山分校统计与运筹学系的Hongtu Zhu课题组2023年6月2日在Science发表的一篇文章讨论了这个问题。他们分析了UK Biobank和BioBank Japan的超过4万名参与者的MRI成像和基因数据,通过大规模统计分析,作者揭示了心脏和大脑的结构和功能之间的相关性,例如心脏成像的特定特征与神经精神疾病之间的联系。具体而言,他们分析了 6 个类别的 82 个心脏和主动脉 MRI 衍生特征:左心室和右心室、左心房和右心房以及升主动脉和降主动脉,以及 458 个测量结构和功能的大脑 MRI 特征。
他们发现心脏的左心室与大脑白质束的微观结构指标具有最强的相关性,表明不良的心脏特征与较差的白质微观结构有关。他们也对心脏 MRI 特征的全基因组进行了关联分析(GWAS),确定了 80 个相关基因组位点 (P < 6.09 × 10-10)。他们确定了心脏 MRI 特征与各种大脑复杂特征和疾病(如中风、饮食失调、精神分裂症、认知功能和心理健康特征)之间的遗传相关性。例如,不利的心肌壁厚度状况与中风呈正相关。该工作也使用双样本孟德尔随机化来探索心脏和大脑之间的因果遗传联系,表明不良心脏特征对精神疾病和抑郁症等多种脑部疾病具有遗传因果影响。
♦ 多组学分析揭示皮肤疤痕形成和创面愈合再生的不同分子事件

图源:论文截图
图源:论文截图
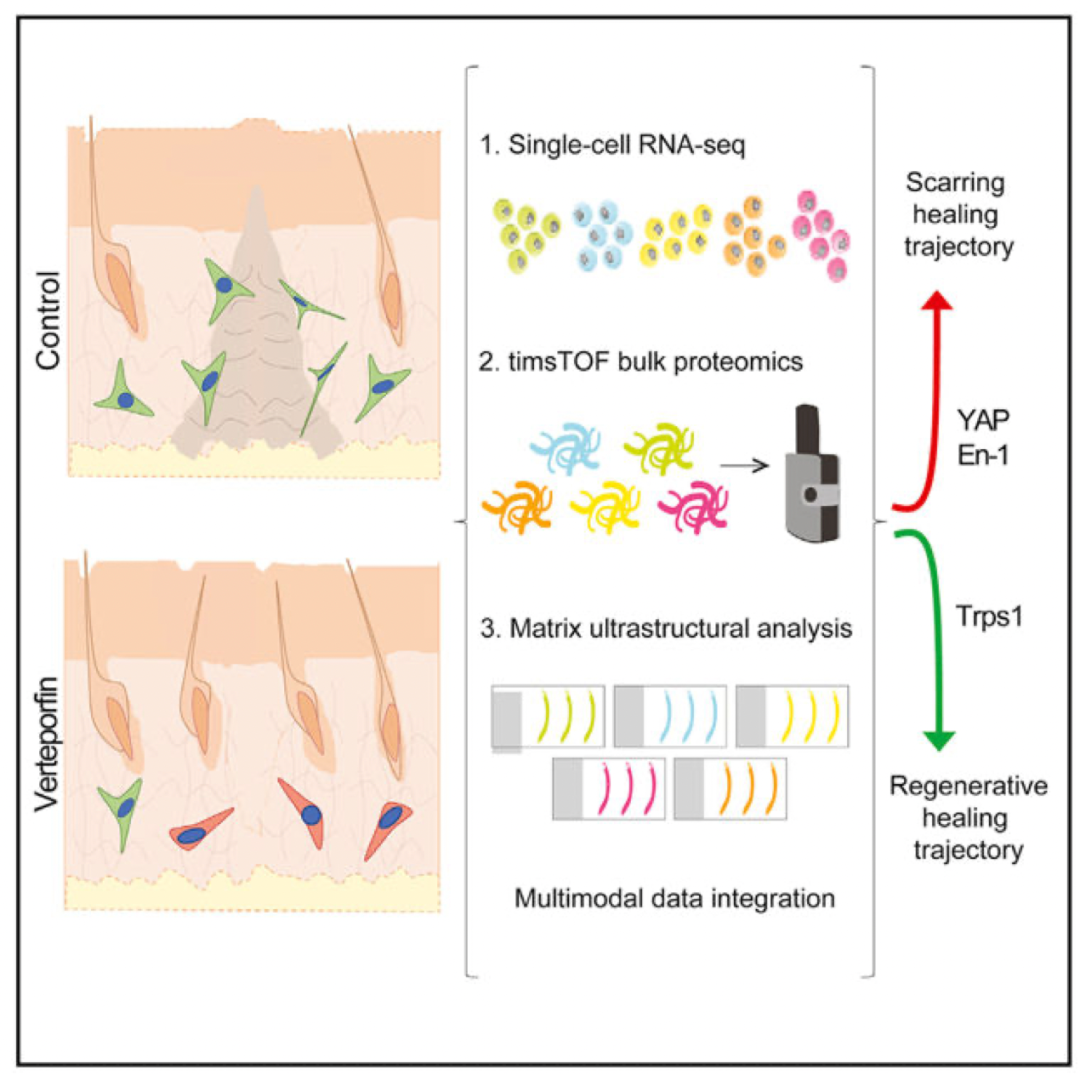
团队报道了驱使皮肤创伤细胞走向瘢痕形成或再生命运的不同分子事件。团队在转录(单细胞RNA测序)、蛋白质组学和组织(细胞外基质超微结构分析)水平上对瘢痕形成与YAP抑制诱导的创面再生进行了分析,以揭示皮肤创面纤维化和再生修复的“分子轨迹”。
研究发现,激活成纤维细胞Trps1和Wnt的信号通路、阻止YAP机械转导促进再生修复。通过在创面中的体内基因敲低和过表达,确定Trps1是再生必需的关键调控基因。本研究为皮肤创面再生修复提供了一个多组学图谱,对组织器官病理性纤维化治疗的探索具有重要意义。
♦ 单细胞深度视觉蛋白质组学(scDVP)

图源:论文截图
Mann在ASMS2023上带来了精彩的单细胞深度视觉蛋白质组学(scDVP)报告,这次演讲的主要工作的去年已经发表在bioRxiv,目前为正在修改的状态。他们在新鲜鼠肝组织样本单shape也就是单细胞鉴定到了1700个蛋白,并在空间上进行热图可视化绘制后发现了ammonia fixation作为一个重要通路。
他们也在不到100个样本上进行了5分类基于随机森林的机器学习模型的构造,并取得了R=0.8的分类效果。还未有演讲更深入的AI算法,就进入到了他们的mDIA技术,意思为在ion mobility层面进行淌度选择后实现multiplexDIA来提升灵敏度实现对单细胞的测量。另外他们还采用了cellenONE ionopticks和astral质谱,实现了对10个shape的测量,但是只能达到约1500个蛋白的鉴定量,也使用了CA-125作为标记物来展示它们的动态范围。
♦ 肿瘤内异质性图谱

图源:论文截图
2023年4月以色列魏茨曼科学研究所的Itay Tirosh团队在Nature上发表题为Hallmarks of transcriptional intratumour heterogeneity across a thousand tumours 的文章,该文章整理、注释和整合了来自77项不同研究的scRNA-seq数据,以揭示覆盖24种肿瘤类型的1163个肿瘤样本的转录ITH(intratumour heterogeneity,ITH)模式。
在恶性细胞中,通过分析各个肿瘤内部基因异质表达模式的相似与不同之处,研究人员基于这些表达程序在不同肿瘤的肿瘤细胞亚群的重复协同上调状态及其发挥的功能聚类这些“共用异质表达程序”,分成了41种meta-programs,以及进一步11种肿瘤内转录异质特征(包括细胞周期、细胞应激等)。
这 41 个共有meta-programs,每个meta-programs由数十个基因组成,这些基因在许多肿瘤的细胞亚群中协调上调。meta-programs涵盖多种细胞过程,包括映射到转录 ITH 的 11 个标志的通用(例如,细胞周期和压力)和谱系特定模式。大多数癌细胞的meta-program与在非恶性上皮细胞中发现的那些相似,这表明很大一部分恶性 ITH 程序甚至在肿瘤发生之前就已经发生变化,反映了它们起源细胞的生物学特性。进一步将meta-program分析扩展到六种常见的非恶性细胞类型,并利用它们来绘制肿瘤微环境中的细胞间相互作用图。
♦ 空间分辨CRISPR筛选平台

图源:论文截图
2023年6月1日,慕尼黑大学Veit Hornung团队和马普所Matthias Mann团队在bioRxiv在线发表了”SPARCS, a platform for genome-scale CRISPR screening for spatial cellular phenotypes“。该文章开发了一个空间分辨CRISPR筛选(spatially resolved CRISPR screening, SPARCS)平台,利用显微镜在包含千万级别细胞的全基因组筛选文库中,物理分离不同表型细胞,实现对空间细胞表型的基因筛选。
作者首先生成了一个U2OS细胞文库表达Brunello CRISPR文库中77,441个sgRNAs,并测试了在PBS膜上对该CRISPR-U2OS细胞库进行1000个细胞核的在体显微切割,测序鉴定了其中平均549个sgRNAs,表明LMD分离细胞核用于CRISPR基因分型的可行性。随后作者构建稳定表达mCherry标记的LC3B(自噬关键蛋白)U2OS细胞,并用mTOR抑制剂Torin-1处理模拟饥饿来诱导自噬模型,通过基于深度学习的图像分类器1.0来区分Torin-1处理和未处理的mCherry-LC3 U2OS细胞,实现了< 1%的错误发现率(FDR)。
为了验证SPARCS对自噬形成相关基因分型的作用,作者构建了转染 Brunello CRISPR KO文库的120万个mCherry-LC3 U2OS细胞库 ,在Torin-1刺激下,通过SPARCS及分类器1.0分离了被分类为自噬关闭的前0.1%细胞,在这些细胞中,靶向参与自噬相关基因(比如ATG5)的sgRNA被高度富集,证明了SPARCS的有效性。为了改进分类器在识别自噬关闭细胞表现不佳的情况,作者通过改进染色和成像方案,训练了分类器2.0,并在包含千万级细胞的全基因组筛选中,进一步改进得到分类器2.1。
♦ 心脑相关性:MRI图像和基因数据的统计分析

图源:论文截图

图源:论文截图
心血管疾病与神经和精神疾病相关,而它们之间的因果联系并没有确定:可能是是由先天易感性引起的也可能是由身体状况引起的压力引起的。
来自北卡罗来纳州教堂山分校统计与运筹学系的Hongtu Zhu课题组2023年6月2日在Science发表的一篇文章讨论了这个问题。他们分析了UK Biobank和BioBank Japan的超过4万名参与者的MRI成像和基因数据,通过大规模统计分析,作者揭示了心脏和大脑的结构和功能之间的相关性,例如心脏成像的特定特征与神经精神疾病之间的联系。具体而言,他们分析了 6 个类别的 82 个心脏和主动脉 MRI 衍生特征:左心室和右心室、左心房和右心房以及升主动脉和降主动脉,以及 458 个测量结构和功能的大脑 MRI 特征。
他们发现心脏的左心室与大脑白质束的微观结构指标具有最强的相关性,表明不良的心脏特征与较差的白质微观结构有关。他们也对心脏 MRI 特征的全基因组进行了关联分析(GWAS),确定了 80 个相关基因组位点 (P < 6.09 × 10-10)。他们确定了心脏 MRI 特征与各种大脑复杂特征和疾病(如中风、饮食失调、精神分裂症、认知功能和心理健康特征)之间的遗传相关性。例如,不利的心肌壁厚度状况与中风呈正相关。该工作也使用双样本孟德尔随机化来探索心脏和大脑之间的因果遗传联系,表明不良心脏特征对精神疾病和抑郁症等多种脑部疾病具有遗传因果影响。
♦ 多组学分析揭示皮肤疤痕形成和创面愈合再生的不同分子事件

图源:论文截图

图源:论文截图
团队报道了驱使皮肤创伤细胞走向瘢痕形成或再生命运的不同分子事件。团队在转录(单细胞RNA测序)、蛋白质组学和组织(细胞外基质超微结构分析)水平上对瘢痕形成与YAP抑制诱导的创面再生进行了分析,以揭示皮肤创面纤维化和再生修复的“分子轨迹”。
研究发现,激活成纤维细胞Trps1和Wnt的信号通路、阻止YAP机械转导促进再生修复。通过在创面中的体内基因敲低和过表达,确定Trps1是再生必需的关键调控基因。本研究为皮肤创面再生修复提供了一个多组学图谱,对组织器官病理性纤维化治疗的探索具有重要意义。
♦ 单细胞深度视觉蛋白质组学(scDVP)

图源:论文截图
Mann在ASMS2023上带来了精彩的单细胞深度视觉蛋白质组学(scDVP)报告,这次演讲的主要工作的去年已经发表在bioRxiv,目前为正在修改的状态。他们在新鲜鼠肝组织样本单shape也就是单细胞鉴定到了1700个蛋白,并在空间上进行热图可视化绘制后发现了ammonia fixation作为一个重要通路。
他们也在不到100个样本上进行了5分类基于随机森林的机器学习模型的构造,并取得了R=0.8的分类效果。还未有演讲更深入的AI算法,就进入到了他们的mDIA技术,意思为在ion mobility层面进行淌度选择后实现multiplexDIA来提升灵敏度实现对单细胞的测量。另外他们还采用了cellenONE ionopticks和astral质谱,实现了对10个shape的测量,但是只能达到约1500个蛋白的鉴定量,也使用了CA-125作为标记物来展示它们的动态范围。
♦ 肿瘤内异质性图谱

图源:论文截图
2023年4月以色列魏茨曼科学研究所的Itay Tirosh团队在Nature上发表题为Hallmarks of transcriptional intratumour heterogeneity across a thousand tumours 的文章,该文章整理、注释和整合了来自77项不同研究的scRNA-seq数据,以揭示覆盖24种肿瘤类型的1163个肿瘤样本的转录ITH(intratumour heterogeneity,ITH)模式。
在恶性细胞中,通过分析各个肿瘤内部基因异质表达模式的相似与不同之处,研究人员基于这些表达程序在不同肿瘤的肿瘤细胞亚群的重复协同上调状态及其发挥的功能聚类这些“共用异质表达程序”,分成了41种meta-programs,以及进一步11种肿瘤内转录异质特征(包括细胞周期、细胞应激等)。
这 41 个共有meta-programs,每个meta-programs由数十个基因组成,这些基因在许多肿瘤的细胞亚群中协调上调。meta-programs涵盖多种细胞过程,包括映射到转录 ITH 的 11 个标志的通用(例如,细胞周期和压力)和谱系特定模式。大多数癌细胞的meta-program与在非恶性上皮细胞中发现的那些相似,这表明很大一部分恶性 ITH 程序甚至在肿瘤发生之前就已经发生变化,反映了它们起源细胞的生物学特性。进一步将meta-program分析扩展到六种常见的非恶性细胞类型,并利用它们来绘制肿瘤微环境中的细胞间相互作用图。









